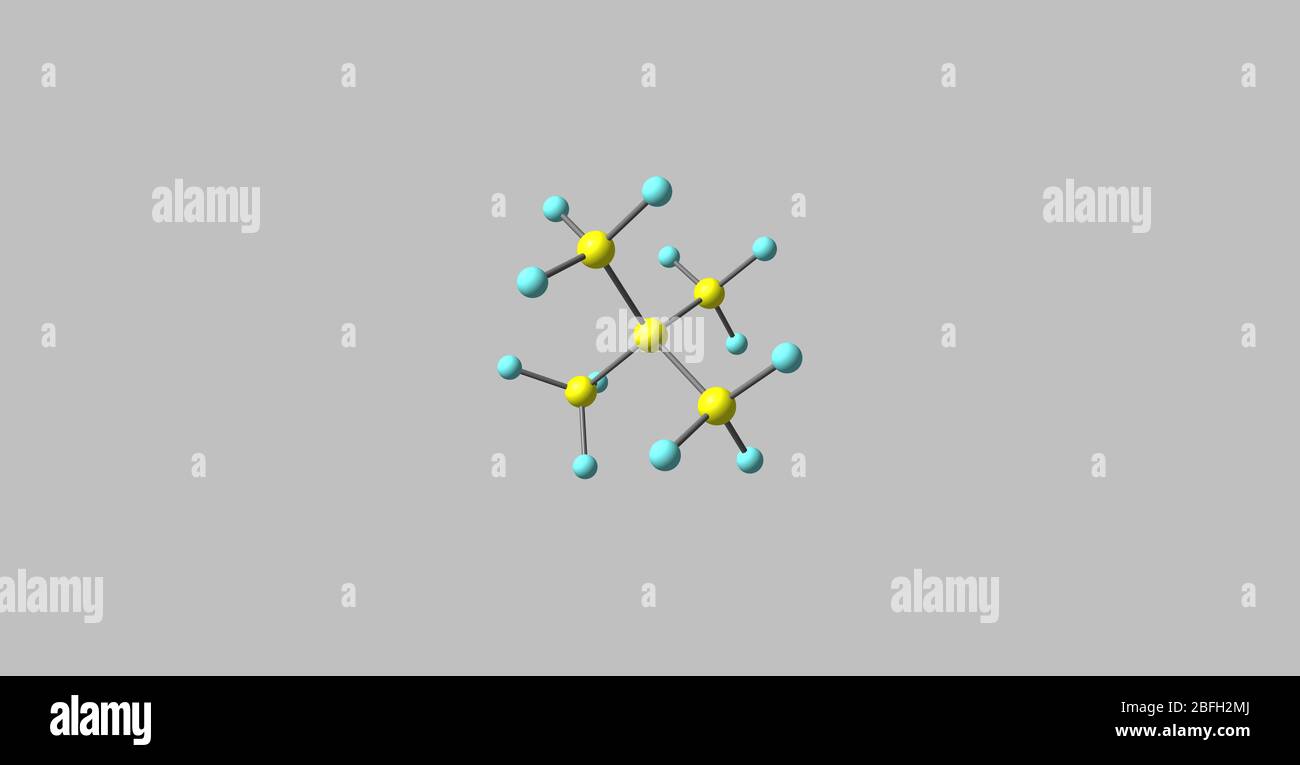
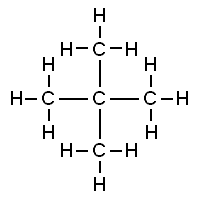
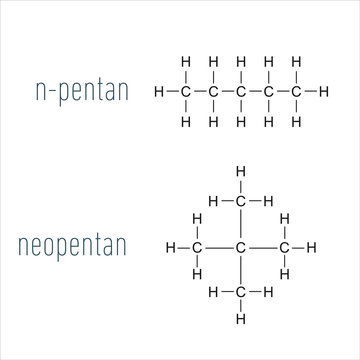
Il neopentano, noto anche come tetrametilmetano, ma avente nome sistematico dimetilpropano e nome IUPAC 2,2-dimetilpropano, è un idrocarburo saturo (alcano) ed è uno dei tre isomeri strutturali del pentano, insieme a n-pentano e isopentano; la sua formula molecolare è C5H12.
La sua formula semistrutturale, che è più indicativa, è C(CH3)4. Questa, che a volte viene anche scritta CMe4, fa vedere chiaramente la sua relazione strutturale con il metano (CH4), il più semplice degli idrocarburi e mostra inoltre che il tetrametilmetano è il primo idrocarburo contenente un carbonio quaternario.
Dal neopentano deriva il gruppo funzionale neopentile ((CH3)3CCH2−), un sostituente che si lega con un carbonio primario e che però si mostra notevolmente ingombrato in alcune reazioni.
In laboratorio venne sintetizzato per la prima volta nel 1870 dal chimico russo Mikhail Lvov. Il nome neopentano fu coniato dal chimico inglese William Odling nel 1876.
Proprietà e struttura molecolare
A temperatura ambiente e pressione atmosferica si presenta come un gas incolore (tecnicamente, un vapore) altamente infiammabile, che in giornate fredde può condensare in un liquido molto volatile dal debole odore gradevole, simile a quello del butano.
Il tetrametilmetano è un composto stabile, la sua formazione dagli elementi è esotermica, ΔHƒ° = -167,9 kJ/mol, ed è il più stabile dei tre isomeri del pentano.
La molecola del tetrametilmetano è tetraedrica, altamente simmetrica: gruppo puntuale Td, e quindi il suo momento dipolare è nullo. Il carbonio centrale e gli altri quattro dei gruppi metilici ad esso uniti sono ibridati sp3. La struttura molecolare del tetrametilmetano è stata indagata con la tecnica della diffrazione elettronica in fase gassosa e dall'analisi dei dati è stato possibile ricavare lunghezze (r) ed angoli (∠) di legame; alcuni dati salienti sono qui riportati (Cc = C centrale; CMe = C metilico):
r(Cc–CMe) = 153,7 pm; r(CMe–H) = 111,4 pm;
∠(Cc−CMe−H) = 112,2°; ∠(H−CMe−H) = 106,6°;
r(CMe … CMe) = 250,8 pm;
Il legame C−C ha la lunghezza corrispondente al suo valore normale (154 pm), mentre il legame C−H è appena più lungo (109 pm).
L'angolo C−C−C è ovviamente di 109,5°; l'angolo Cc−CMe−H è più ampio del valore ottimale per l'ibridazione sp3, 109,5°, mentre l'angolo H−CMe−H è più stretto.
La distanza tra due carboni metilici è inferiore al doppio del raggio di van der Waals del carbonio (170 pm) e ancor più inferiore a quello stimato per il gruppo metilico (200 pm).
L'elevata simmetria della molecola ha conseguenze entropiche sui livelli rotazionali della molecola, che hanno l'effetto di innalzare notevolmente i suoi punti di fusione (−16,4 °C) ed ebollizione (9,50 °C) rispetto ai corrispondenti valori dell'isomero lineare (n-pentano, -129,7°C e 36,1°C).
La simmetria perfettamente tetraedrica ha anche come conseguenza il fatto che i 12 atomi di idrogeno producano un unico segnale (un singoletto) a δ = 0,902 ppm nello spettro di risonanza magnetica nucleare protonica in soluzione di tetraclorometano.
Sintesi
Il neopentano è presente nel petrolio greggio e da questo può essere estratto.
Un metodo di sintesi del neopentano è basato su una reazione tra il dimetilzinco e il cloruro di t-butile, o anche il bromuro o ioduro:
(CH3)3CCl CH3−Zn−CH3 → (CH3)4C Cl−Zn−CH3
Similmente, è riportata la reazione tra lo ioduro di t-butilmagesio con il dimetilsolfato in etere:
(CH3)3C−Mg−I (CH3−O)2SO2 → (CH3)4C CH3−O−SO2−O−Mg−I
Note
Voci correlate
- n-pentano
- Isopentano
- Metano
Altri progetti
- Wikimedia Commons contiene immagini o altri file su neopentano